(ch. clin. i-STAT) CONTROLE PT/INR niv. 1, kit, 5+5 06P17-13
Outdated Article
(chimie clinique i-STAT) KIT CONTROLES PT/INR
Définition
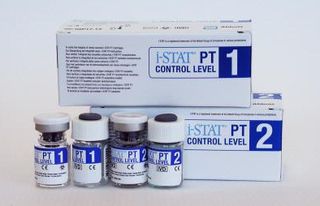
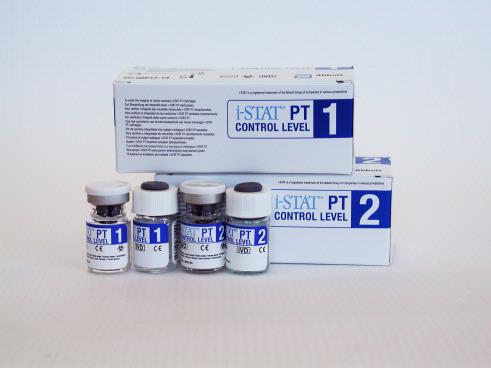
Solution de contrôle à utiliser avec la cartouche i-STAT PT/INR. Niveau 1 est normal et Niveau 2 est anormal.
Spécifications
Spécifications techniques
Les contrôles i-STAT PT, niveau 1 et 2, sont contenus dan sdes flacons de 6 ml. Des flacons séparés de 6 ml contiennent 1 à 3 ml de solution de chlorure de sodium pour la reconstitution.
Emballage et étiquetage
Chaque niveau de contrôle est composé de 5 flacons de plasma humain lyophilisé + 5 flacons de diluant de' chlorure de sodium (9,5 +/- 1,5 mmol/l)
Conseils d'utilisation
Veuillez consulter les ‘Procédures de laboratoire mises à jour, 2022' disponibles en ligne via la page sharepoint du Groupe de travail du Laboratoire : Procédures et Ressources de Laboratoire
https://msfintl.sharepoint.com/sites/msfintlcommunities/LabWG/SitePages/Laboratory-Manual-page.aspx
Pour accès hors ligne, contactez votre référent de laboratoire.
Conservation
- Au réfrigérateur entre 2 et 8ºC
- Ne pas congeler
- Durée de conservation: 12 mois
- Durée de conservation minimum garantie à la livraison: 1/3 de la durée totale de conservation
- Les solutions de contrôles peuvent être conservées à température ambiante (18 à 30°C) jusqu'à 4 heures
- Ne pas conserver une solution de contrôle reconstituée. La solution doit être utilisée immédiatement.
Gestion des Déchets
Eliminer ce produit comme un déchet biologique dangereux, selon les régulations locales, régionales et nationales

![[ELAECCHT107] (chimie clinique i-STAT) CARTOUCHE COAGULAT. PT/INR 03P89-24](/web/image/product.template/571429/image_256/%5BELAECCHT107%5D%20%28chimie%20clinique%20i-STAT%29%20CARTOUCHE%20COAGULAT.%20PT-INR%2003P89-24?unique=25cbff4)